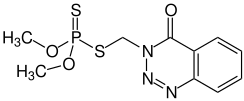
أزينفوز-ميثيل
أزينفوز-ميثيل أو أزينوفوز - ميثيل أو جوثيون هو مركب فوسفات عضوي تصنعه عدة شركات من بينها باير كروبساينس، وغوان كو، وماختشيم أغان،[4] ويستعمل كمبيد حشري واسع الطيف.
| أزينفوز-ميثيل | |
|---|---|
| التسمية المفضلة للاتحاد الدولي للكيمياء البحتة والتطبيقية | |
O,O-Dimethyl S-[(4-oxo-1,2,3-benzotriazin-3(4H)-yl)methyl] phosphorodithioate |
|
| أسماء أخرى | |
أزينفوز-ميثيل، وأزينوفوز - ميثيل، وغوثيون |
|
| المعرفات | |
| الاختصارات | AZM |
| رقم CAS | 86-50-0 |
| بوب كيم (PubChem) | 2268 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
|
|
| الخواص | |
| صيغة كيميائية | C10H12N3O3PS2 |
| كتلة مولية | 317.32 غ.مول−1 |
| المظهر | بلورات لها لون برتقالي شاحب أو داكن أو شفاف |
| الكثافة | 1.44 g cm−3 |
| نقطة الانصهار | 73 °س، 346 °ك، 163 °ف |
| نقطة الغليان | 200 °س، 473 °ك، 392 °ف |
| الذوبانية في الماء | 28 mg dm−3 |
| log P | 2.466 |
| ضغط البخار | 8 x 10−9 ملليمتر زئبق[1] |
| المخاطر | |
| رمز الخطر وفق GHS |   [2] [2] |
| وصف الخطر وفق GHS | Danger |
| بيانات الخطر وفق GHS | H300, H311, H317, H330, H410[2] |
| بيانات وقائية وفق GHS | P260, P264, P273, P280, P284, P301+310[2] |
| NFPA 704 |
|
| حد التعرض المسموح به U.S | TWA 0.2 mg/m3 [skin] |
| LD50 | 16 mg/kg (rat, oral) 80 mg/kg (guinea pig, oral) 11 mg/kg (rat, oral) 13 mg/kg (rat, oral) 8.6 mg/kg (mouse, oral) 7 mg/kg (rat, oral) 8 mg/kg (mouse, oral) 10 mg/kg (dog, oral)[3] |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
يدين الأزينفوز-ميثيل، مثل مبيدات الآفات الأخرى التي تنتمي لنفس الفئة، بخصائصه كمبيد حشري (ومادة سامة للإنسان) لحقيقة أنه مثبط لأستيل الكولين إستراز، وهي ذات الآلية المسؤولة عن التأثيرات السامة للأسلحة الكيميائية كغاز الأعصاب من السلسلة V.
يُصنف الأزينفوز-ميثيل باعتباره مادة شديدة الخطورة في الولايات المتحدة الأمريكية على النحو المحدد في القسم 302 من قانون التخطيط للطوارئ وقانون حق المجتمع في المعرفة (42 U.S.C. 11002)، وتخضع المنشآت التي تنتج وتخزن أو تستخدم الأزينفوز-ميثيل بكميات كبيرة لرقابة صارمة.[5]
لمحة تاريخية
عدلطور الأزينفوز-ميثيل لأول مرة خلال الحرب العالمية الثانية كأحد السموم العصبية المشتقة من عوامل الأعصاب،[4] وسُجل للاستخدام كمبيد حشري لأول مرة في الولايات المتحدة الأمريكية في عام 1959، واستخدم أيضًا كعنصر نشط في مبيدات الفوسفات العضوي (OP)،[6] ولكنه لم يُتح للاستخدام الاستهلاكي في المنازل والبيئات السكنية حيث ارتبط الأزينفوز-ميثيل بالمشاكل الصحية للمزارعين الذين يستخدمونه، ورفضت وكالة حماية البيئة الأمريكية إعادة الترخيص باستخدامه بسبب المخاوف من خطورة تأثيره الضار على عمال المزارع، ومستخدمي مبيدات الآفات، والنظم البيئية المائية.[4] حُظر استخدام أزينفوز-ميثيل بشكل كامل في الولايات المتحدة الأمريكية في 30 سبتمبر 2013، وقد سبقت إجراءات التخلص التدريجي من الأزينفوز-ميثيل ذلك بنحو اثني عشر عامًا.[7] كما حُظر الأزينفوز-ميثيل في دول الاتحاد الأوروبي منذ عام 2006،[8] وفي تركيا منذ عام 2013.[6] وقد اتخذت هيئة إدارة المخاطر البيئية النيوزيلندية قرارًا بالتخلص التدريجي من الأزينفوز-ميثيل خلال فترة خمس سنوات بدءًا من عام 2009.[9] ظل الأزينفوز-ميثيل قيد الاستخدام في أستراليا، وجزئيًا في نيوزيلندا حتى عام 2014.[6]
الأنواع المتوفرة
عدلغالبًا ما يستخدم الأزينفوز-ميثيل كمكون نشط في مبيدات الفوسفات العضوية مثل غوثيون وغوساثيون، وغوساثيون - م، وكوتنيون، وكريسثيون، وكوتنيوم ميثيل، والكارفين، وميتريلتريزوشن، وباي 9028، وباي 17147، وآر - 1852. وهذا هو السبب وراء استخدام اسم غوثيون في بعض الأحيان للإشارة إلى الأزينفوز-ميثيل غالبًا. أظهرت الدراسات أن مبيد الأزينفوز-ميثيل النقي أقل سمية من مبيد الغوساثيون، ويمكن أن تعزى سمية الأزينفوز-ميثيل المتزايدة هذه إلى التفاعلات التي تحدث بين المركبات المختلفة في الخليط.[6]
التحضير
عدليمكن تحضير الأزينفوز-ميثيل من خلال سلسلة من الخطوات:
- تتم تنقية مركب الأو - نيتروأنيلينلين o-nitroaniline من خلال الذوبان في خليط الماء الساخن والإيثانول بالنسبة إلى 2: 1.، ثم يضاف الكربون النشط وترشح النتيجة للتوضيح.
- يتم تبريد المادة المرشحة أثناء الحركة لتوليد البلورات عادةً عند 4 درجات مئوية، ولكن إذا لزم الأمر يمكن تبريدها أيضًا حتى -10 درجة مئوية. ثم يتم جمع البلورات وغسلها وتجفيفها.
- يستخدم الخليط إذا كان نقيًا بدرجة كافية لفي الخطوات التالية، والتي تتم عند درجة حرارة تتراوح من 0 إلى 5 درجات مئوية.
- لإنتاج الأو - نيتروبنزونيتريل - 14 سي o-Nitrobenzonitrile-14C، يوضع المكون الأول، وهو الأوكسي - نيتروأنيلين مع الثلج والماء.
- يضاف نتريت الصوديوم المذاب في الماء إلى هذا الخليط الرقيق.
- بعد تكوين محلول أصفر شاحب، والذي يشير إلى اكتمال تفاعل الديازوتيز، ينبغي تعديل الأس الهيدروجيني إلى 6، ويتم بعد ذلك إدخال المحلول إلى خليط من سيانيد النحاس والتولوين.
- تُزال طبقة التولوين في درجة حرارة الغرفة، ثم تغسل الطبقة المائية وتجفف ويعزل الناتج المنقى عن طريق التبلور، ويكون الناتج الثالث هو الأنثرانيلاميد -14 سي.
- يتكون الـo-Nitrobenzonitrile-14C، والذي يتم حله أولاً في الإيثانول وهيدرات الهيدرازين.
- يتم تسخين المذيب لاحقًا، ومعالجته في غطاء جيد التهوية بشحنات دورية صغيرة، أقل من 10 مجم من نيكل راني.
- تتم تصفية المحلول الإيثانولي وتجفيفه في جو من النيتروجين.
- الخطوة التالية هي تكوين 1،2،3-بنزوتريازين -4 (3H) -one-14C (وهو المركب الرابع).
- يضاف نتريت الصوديوم المذاب في الماء إلى أنثرانيلاميد وحمض الهيدروكلوريك في الماء المثلج.
- يتكون ناتج ذو لون أصفر شاحب مرة أخرى كرد فعل ديازوتيزي.
- بعد ذلك يتم ضبط الأس الهيدروجيني إلى 8.5، ويتسبب هذا في إغلاق الحلقة لتشكيل 1،2،3-بنزوتريازين -4 (3H) -one-14C.
- ينتج عن هذا محلول ملح الصوديوم الذي يمكن معالجته بحمض الهيدروكلوريك، مما يخفض الرقم الهيدروجيني إلى 2 حتى 4.
- يتم جمع بلورات 1،2،3-بنزوتريازين -4 (3H) -one-14C وغسلها وتجفيفها.
- لتكوين 1،2،3-بنزوتريازين-4- (3-كلورو ميثيل) -ون -14 ج تتم إضافة 1،2،3-بنزوتريازين -4 (3H) -one-14C والبارافورمالدهيد إلى ثنائي كلوريد الإيثيلين وتسخينها إلى 40 درجة مئوية.
- يضاف كلوريد الثيونيل ويسخن المذيب بالكامل إلى 65 درجة مئوية، وبعد أربع ساعات من التسخين يُبرد المحلول إلى درجة حرارة الغرفة، ثم يضاف الماء ويتم تحييد المحلول.
- تُزال طبقة ثنائي كلوريد الإيثيلين ويتم تجميعها مع نتيجة الطبقة المائية المغسولة، ثم يرشح المذيب ويجفف.
- أخيرا يتم التحضير الفعلي للأزينفوز-ميثيل بإضافة ثنائي كلوريد الإيثيلين إلى المركب الناتج من الخطوة الخامسة، 1، 2، 3-بنزوتريازين-4- (3-كلورو ميثيل) -ون -14 ج، ثم يسخن هذا الخليط إلى 50 درجة مئوية ويضاف بيكربونات الصوديوم وملح الصوديوم ثنائي ميثيل فوسفوروديثيونات الصوديوم في الماء.
- تزال طبقة ثنائي كلوريد الإيثيلين وتتم إعادة استخلاصها باستخدام ثنائي كلوريد الإيثيلين وتنقيتها بالترشيح، ثم يجفف المرشح النقي.
- تتم تنقية هذا الناتج مرة أخرى عن طريق إعادة التبلور من الميثانول، ويكون ما تبقى هو أزينفوز-ميثيل نقي على شكل بلورات بيضاء.[10]
الامتصاص
عدليمكن للأزينفوس-ميثيل دخول الجسم عن طريق الاستنشاق، أو الابتلاع، أو التلامس المباشر عن طريق الجلد.[11] يوتعرض جزء كبير من السكان لجرعات منخفضة من الأزينفوز-ميثيل بسبب وجودها كمخلفات في الطعام ومياه الشرب. يمكن امتصاص الأزينفوز-ميثيل في الجهاز الهضمي بعد ابتلاعه مباشرة،[12] كما يمكن للأزينفوز-ميثيل أيضًا أن يدخل الجسم من خلال خلايا الجلد عند ملامسته مباشرة عن طريق الجلد.[11] ويعد الامتصاص عن طريق الجلد مسؤولاً عن تعرض أكثر مستخدمي الأزينفوز-ميثيل المهنيين لجرعات عالية نسبيًا منه، وخاصة العمال الزراعيين.[12]
آلية التأثير السام
عدليمكن أن يسبب الأزينفوز-ميثيل بمجرد امتصاصه تأثيرات سامة للأعصاب، مثله في ذلك مثل المبيدات الحشرية الفوسفاتية العضوية الأخرى.[13] يمكن أن يكون الأزينفوز-ميثيل نفسه سامًا عند التركيزات العالية لأنه يمكن أن يعمل كمثبط لأسيتيل الكولين إاستراز، إلا أن سُميته ترجع أساسًا إلى السيتوكروم الذي يعمل على تنشيطه حيويا بنزع الكبريت وتحويله إلى مركب ثلاثي الفوسفات أو الأوكسون.[12] يمكن أن يتفاعل مبيد غوتوكسون مع مجموعة هيدروكسيل السيرين في الموقع النشط لأسيتيل الكولين إستراز، ثم يحجب الموقع النشط ومن ثم يعطل وصول أسيتيل الكولين استراز. يعمل أستيل الكولين استراز في الظروف العادية على تحلل سريع وفعال للناقل العصبي لأستيل الكولين، وبالتالي إنهاء النشاط الحوي للأستيل الكولين. ويؤدي تثبيط إنزيم أسيتيل الكولين استراز إلى إحداث تراكم فوري للإنزيم مما يؤدي في النهاية إلى تحفيز مفرط للجهاز العصبي.[13]
طرق التخلص من التأثير السام
عدليمكن تحويل الأزينفوز-ميثيل حيويا لمنع تأثيراته السامة. فكما يمكن تنشيطه حيويًا من خلال إزالة الكبريت بوساطة السيتوكروم الذي يحوله إلى مركب ثلاثي الفوسفات أو الأوكسون، فإنه من الممكن أيضًا إزالة سميته باستخدام السيتوكروم أيضا.[12] يحفز السيتوكروم الانقسام التأكسدي لرابطة الكبريت P-S-C في الأزينفوز-ميثيل. تتضمن المسارات الأخرى لإزالة سمية الأزينفوز-ميثيل عملية إزالة الألكلة باستخدام الغلوتاثيون عبر انقسام للرابطة P-O-CH3، والتي تشكل الأزينفوز-ميثيل أحادي الميثيل وGS-CH3. يمكن إزالة الميثيل الأحادي هذا من الأزينفوز-ميثيل أحادي الميثيل وتحويله إلى أزينفوز-ميثيل ثنائي الميثيل وGS-CH3 مرة أخرى.
قد يخضع الأزينفوز-ميثيل أيضًا لعملية إزالة الأحماض الدهنية المحفزة بالغلوتاثيون. ويمكن إزالة السموم من الغوتوكسون مرة أخرى باستخدام السيتوكروم الذي يعمل على تحفيز الانقسام التأكسدي للغوتوكسون. تتضمن مسارات إزالة السموم الأخرى من الغوتوكسون عملية نزع الألكلة باستخدام الغلوتاثيون، والذي يمر عبر انقسام رابطة P-O-CH3 لتكوين أزينفوز-ميثيل وGS-CH3 منزوع الميثيل.[14][15][16]
العلامات الحيوية على التعرض للأزينفوز-ميثيل
عدليعد تثبيط أسيتيل الكولين استراز هو أكثر العلامات الحيوية شيوعًا للتعرض للأزينفوز-ميثيل. كما يعمل الأزينفوز-ميثيل على تثبيط إنزيمات الإستراز الأخرى مثل البوتريل كولين إستراز. ويمكن بشكل عام اكتشاف التعرض للأزينفوز-ميثيل بشكل أفضل حين يحدث تثبيط لأسيتيل الكولين استراز. يعد تثبيط أسيتيل الكولين استراز في البرمائيات وأسماك الزرد أيضًا علامة حيوية أكثر حساسية لمستويات التعرض المنخفضة للأزينفوز-ميثيل.[6] يمكن استقلاب الأزينفوز-ميثيل كما ذكرنا سلفا إلى ألكيل فوسفات ثنائي الميثيل غير سام باستخدام السيتوكروم والغلوتاثيون. وتتمثل ألكيلات الفوسفات ثنائية الميثيل غير السامة هذه في مركبات ثنائي ميثيل الفوسفات، وثنائي ميثيل الثيوفوسفات، وثنائي ميثيل ثنائي الثيوفوسفات، تفرز هذه المستقلبات الثلاثة في البول ويمكن استخدامها كمؤشرات حيوية موثوقة للدلالة على التعرض لمستويات من الفوسفات. بيد أن هذه المستقلبات ليست خاصة فقط بالأزينفوز-ميثيل، لأن مبيدات الآفات الفوسفاتية العضوية الأخرى قد يتم استقلابها أيضًا في مركبات الألكيل فوسفات الثلاثة. يمكن أيضًا استخدام كمية أسيتيل الكولين استراز في كرات الدم الحمراء في الدم كمؤشر حيوي لتأثير الأزينفوز-ميثيل.
يعد مستوى أسيتيل الكولين استراز في خلايا الدم الحمراء في الدم هو أفضل مؤشر على نشاط أسيتيل الكولين استراز في المشبك العصبي، لأنه يوازي بشكل وثيق مستوى اسيتيل الكولين استراز الموجود في الجهاز العصبي المركزي والجهاز العصبي المحيطي. يرتبط انخفاض إنزيم اسيتيل الكولين استراز الخاص بخلايا الدم الحمراء بالتأثيرات الناتجة عن التثبيط السريع لأنزيمات اسيتيل الكولين استراز الموجودة في الأنسجة الأخرى، ويرجع ذلك إلى حقيقة أن كلا الإنزيمين يمكن أن يعمل الأزينفوز-ميثيل على تثبيطها.[13]
طرق العلاج
عدلهناك آليتان رئيسيتان مختلفتان لعلاج التسمم بمادة الأزينفوز-ميثيل. تتمثل إحدى هاتين الآليتين في علاج المريض قبل التعرض للأزينفوز-ميثيل، بينما تتمثل الآخرى في علاج المريض بعد حدوث التسمم. يمكن استخدام المضادات التنافسية لأسيتيل الكولين استراز في المعالجة المسبقة. ويمكن أن تقلل من معدل الوفيات الناجم عن التعرض للأزينفوز-ميثيل، حيث يمكن أن نجعل مثبطات أسيتيل الكولين استراز العضوية الفسفورية ترتبط مؤقتًا بالموقع التحفيزي للإنزيم.[17] بسبب هذا الارتباط، لا يستطيع الأزينفوز-ميثيل فسفرة الإنزيم بعد ذلك ويكون تثبيط الإنزيم أقصر.[17]
تتمثل آلية العلاج بعد التعرض لتسمم الأزينفوز-ميثيل في منع تنشيط المستقبل المسكاريني. تستخدم مضادات الاختلاج للسيطرة على النوبات العصبية وتستخدم الأوكسيم لإعادة تنشيط أسيتيل الكولين استراز المثبط.[17] تقوم الأوكسيمات بإزالة مجموعة الفوسفوريل المرتبطة بالموقع النشط لأسيتيل الكولين استراز عن طريق الارتباط بها.[18] هناك عدد قليل من الأوكسيمات الأكثر فاعلية في علاج تسمم أزينفوز-ميثيل، وهي الأوكسيم K-27 والفيزوستيغمين.[17] يستخدم كلا هذين العلاجين معًا أيضًا، حيث يتم علاج بعض المرضى باستخدام الأتروبين (وهو مضاد تنافسي لأسيتيل الكولين استراز) وإعادة تنشيط الأوكسيم. ولكن عندما يظهر المريض مقاومة للأتروبين، يمكن علاج المرضى بإعطائه جرعات منخفضة من الأنيسودامين، وهو مضاد للكولين ومضاد للأدرينال ألفا -1، لتحقيق وقت شفاء أقصر.[18] يعتبر العلاج بمزيج من قلويدات مختلفة أو بالتآزر مع الأتروبين أكثر أمانًا من استخدام تركيزات عالية من الأنتروبونين، والتي يمكن أن تكون سامة. يتمثل الاحتمال الآخر في استخدام تقنية المفاعل الحيوي الغشائي. ولا يلزم عند استخدام هذه التقنية إضافة أي مركبات كيميائية أخرى.[19] تعتبر المعالجة المسبقة على أية حال أكثر فاعلية من المعالجة اللاحقة.[17]
التأثيرات الصحية
عدلالتأثيرات المحتملة على الإنسان
عدلتلعب الأعصاب الكولينية دورًا مهمًا في الوظيفة الطبيعية للجهاز العصبي المركزي، والغدد الصماء، والجهاز العصبي المحيطي، وجهاز المناعة، والجهاز التنفسي. ونظرًا لأن جميع الألياف الكولينية تحتوي على تركيزات عالية من أسيتيل الكولين وأسيتيل الكولين استراز في أطرافها، فإن تثبيط أسيتيل الكولين استراز يمكن أن يضعف وظيفتها. لذا فإن التعرض للأزينفوز-ميثيل الذي يثبط الإنزيم المحول للأنغيوتنسين، قد يزعج الكثير من الأنظمة المهمة وقد يكون له تأثيرات مختلفة. ففي الجهاز العصبي اللاإرادي يؤدي تراكم الأسيتيل كولين إلى زيادة تحفيز المستقبلات المسكارينية للجهاز العصبي السمبثاوي.[11][13] يمكن أن يؤثر ذلك على الغدد الصماء الخارجية كأن يؤدي إلى زيادة إفراز اللعاب والعرق والتمزق، وعلى الجهاز التنفسي فيؤدي إلى زيادة الإفرازات القصبية وضيق الصدر والصفير، وعلى الجهاز الهضمي فيؤدي إلى الغثيان والقيء والإسهال، وعلى العينين فيؤدي إلى انقباض الحدقة، وعدم وضوح الرؤية، وعلى الجهاز القلبي الوعائي فيؤدي إلى انخفاض ضغط الدم، وبطء القلب. كما قد يؤدي التحفيز المفرط لمستقبلات النيكوتين في الجهاز العصبي إلى آثار ضارة على الجهاز القلبي الوعائي، مثل الشحوب وعدم انتظام ضربات القلب وزيادة ضغط الدم. أما في العضلات ققد يتسبب تراكم الأستيل كولين في تحزُّم العضلات، والشلل، والتشنجات، ونغمة رخوة أو صلبة. قد يؤدي الإفراط في تحفيز الأعصاب في الجهاز العصبي المركزي، وتحديداً في الدماغ، إلى النعاس والارتباك العقلي والخمول. تشمل التأثيرات الأكثر شدة للأزينفوز-ميثيل على الجهاز العصبي المركزي حدوث حالة من الغيبوبة بدون ردود أفعال، وزراق وحجب في مراكز الجهاز التنفسي.[20] وبالتالي فإن تثبيط إنزيم أسيتيل الكولين استراز قد يكون له تأثيرات مختلفة كثيرة.
التأثيرات المحتملة على الحيوانات
عدلتتضمن الآثار المحتملة للأزينفوز-ميثيل على الحيوانات اضطراب الغدد الصماء والضعف التناسلي وضعف المناعة والسرطان.[21] وهناك ظاهرة ملحوظة تم إثباتها في العديد من الدراسات التي أجريت على الحيوانات وهي أن التعرض المتكرر للفوسفات العضوي يجعل الثدييات أقل عرضة للتأثيرات السامة لمثبطات الإنزيم المحول للأنجيوتنسين، على الرغم من أن أنشطة الكولينستراز تكون غير طبيعية. تكون هذه الظاهرة ناتجة عن زيادة ناهضات الأسيتيل كولين داخل المشابك العصبية، مما يؤدي في النهاية إلى تنظيم سفلي للمستقبلات الكولينية، وبالتالي، يؤدي وجود تركيز معين من الأسيتيل كولين داخل المشبك إلى توفير عدد أقل من المستقبلات، مما يؤدي بعد ذلك إلى استجابة أقل.[13] كما أظهرت الدراسات أن الإنزيم المحول للأنجيوتنسين في أدمغة الأسماك أكثر عرضة للفوسفات العضوي منه في أدمغة البرمائيات. ويمكن تفسير ذلك من خلال تقارب العظم ومعدل فسفرة الإنزيمات. يمتلك دماغ الضفدع على سبيل المثال تقارب عظام أقل للأزينفوز-ميثيل، ومعدل فسفرة أبطأ من أسيتيل كولين الإستراز الموجود في دماغ السمكة.[6]
تتمثل تأثيرات التعرض للأزينفوز-ميثيل على البرمائيات في قلة الحجم، وانثناء الحبل الظهري، وحدوث تصبغ غير طبيعي، وحدوث خلل في القناة الهضمية والخياشيم، والسباحة في دوائر، وتقصير الجسم، وضعف النمو. يعدل الأزينفوز-ميثيل في قنافذ البحر تجميع الهيكل الخلوي بتركيزات عالية، كما يمكن أن يغير ترسب الهيكل العظمي لليرقة بتركيزات منخفضة.[6][22] ويتسبب تعرض الفئران للأزينفوز-ميثيل في فقدان الوزن، حيث يثبط الأزينفوز-ميثيل إنزيم الكولينستراز في الدماغ، ويقلل من استهلاك الفئران للطعام، ويعتبر الانخفاض بنسبة 45-50٪ في معدل الكوليسترول في الدماغ مميتًا في الفئران.[23] يقلل الأزينفوز-ميثيل أيضًا من نشاط الأسيتيل كولين اإستراز في ديدان الأرض والجرذان.[24][25]
توضح مراجع الدراسات التالية بشكل أكثر استفاضة تأثير الأزينفوز-ميثيل على عدد من الحيوانات:
- الزرديات.[26]
- دودة الأرض.[27]
- أسماك البلطي.[28]
- ضفادع شجرة المحيط الهادي، والسمندل المائي.[29]
- العلجوم.[30]
- أسماك سلمون قوس قزح.[31]
- مقارنة بين التأثير في ضفادع أشجار المحيط الهادي والتأثير في أسماك سلمون قوس قزح.[32]
- أسماك البطحيش المرقش.[33]
الانحلال
عدليكون الأزينفوز-ميثيل مستقرًا جدًا عند إذابته في الماء الحمضي أو المحايد أو القلوي قليلاً، ولكن ولكن في حال زيادة الأس الهيدروجيني إلى 11 فإنه يتحلل بسرعة إلى حمض الأنثرانيليك والبنزاميد ومواد كيميائية أخرى. تتسبب الكائنات الحية الدقيقة وأشعة الشمس في البيئات الطبيعية الغنية بالمياه في انحلال الأزينفوز-ميثيل بشكل أسرع، وتكون فترة عمر النصف له متغيرة بشكل كبير بحسب الحالة فتتراوح ما بين عدة أيام وعدة أشهر. يعد التحلل الحيوي والتبخر في ظل الظروف العادية من الطرق الرئيسية لاضمحلال الأزينفوز-ميثيل، إذ يتعرض الأزينفوز-ميثيل بعد التبخر للأشعة فوق البنفسجية بشكل أكبر، مما يسبب التحلل الضوئي. يمكن أن تصل فترة عمر النصف للأزينفوز-ميثيل مع القليل من النشاط الحيوي وعدم التعرض للأشعة فوق البنفسجية إلى حوالي عام.[34]
المراجع
عدل- ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعPGCH - ^ ا ب ج Sigma-Aldrich Co., Azinphos-methyl. Retrieved on 2022-03-17.
- ^ اكتب عنوان المرجع بين علامتي الفتح
<ref>والإغلاق</ref>للمرجعIDLH - ^ ا ب ج "EPA's Interrum Reregistration Eligibility Decision for Azinphos-methyl".
{{استشهاد بدورية محكمة}}: الاستشهاد بدورية محكمة يطلب|دورية محكمة=(مساعدة) - ^ "40 C.F.R.: Appendix A to Part 355—The List of Extremely Hazardous Substances and Their Threshold Planning Quantities" (PDF) (ط. July 1, 2008). مكتب النشر لحكومة الولايات المتحدة. مؤرشف من الأصل (PDF) في 2012-02-25. اطلع عليه بتاريخ 2011-10-29.
{{استشهاد بدورية محكمة}}: الاستشهاد بدورية محكمة يطلب|دورية محكمة=(مساعدة) - ^ ا ب ج د ه و ز Gungordu,A؛ Uckun, M (2014). Comparative assessment of in vitro and in vivo toxicity of azinphos methyl and its commercial formulation. Environ Toxicol.
- ^ "EPA's Azinphos-methyl Page". مؤرشف من الأصل في 2016-03-05. اطلع عليه بتاريخ 2015-04-15.
- ^ Scott، Alex (4 أغسطس 2008). "Europe Rejects Appeal for Use of Azinphos-methyl Pesticide". Chemical Week. مؤرشف من الأصل في 2022-03-14. اطلع عليه بتاريخ 2008-08-11.
- ^ ERMA نسخة محفوظة January 31, 2010, على موقع واي باك مشين. - press release
- ^ White، E.R. (1972). "Synthesis of carbon-14-benzenoidring-labeled Guthion". Journal of Agricultural and Food Chemistry. ج. 20 ع. 6: 1184–1186. DOI:10.1021/jf60184a037.
- ^ ا ب ج Roney.N., C.S.؛ Stevens. Y.W.؛ Quinones-Rivera.A.؛ Wohlers.D؛ Citra.M. (2008). Toxicological Profile For Guthion. U.S. DEPARTMENT OF HEALTH AND HUMAN SERVICES.
- ^ ا ب ج د Buratti، F.M. (2003). "CYP-specific bioactivation of four organophosphorothioate pesticides by human liver microsomes". Toxicol Appl Pharmacol. ج. 186 ع. 3: 143–154. DOI:10.1016/s0041-008x(02)00027-3.
- ^ ا ب ج د ه Carrier, G.؛ R.C. Brunet (1999). "A toxicokinetic model to assess the risk of azinphosmethyl exposure in humans through measures of urinary elimination of alkylphosphates". Toxicol Sci. ج. 47 ع. 1: 23–32. DOI:10.1093/toxsci/47.1.23.
- ^ Levine, B.S.؛ S.D. Murphy (1977). "Effect of piperonyl butoxide on the metabolism of dimethyl and diethyl phosphorothionate insecticides". Toxicol Appl Pharmacol. ج. 40 ع. 3: 393–406. DOI:10.1016/0041-008x(77)90067-9.
- ^ Sultatos, L.G.؛ L. Woods (1988). "The role of glutathione in the detoxification of the insecticides methyl parathion and azinphos-methyl in the mouse". Toxicol Appl Pharmacol. ج. 96 ع. 1: 168–174. DOI:10.1016/0041-008x(88)90259-1.
- ^ Motoyama N, D.W. (1972). The in vitro metabolism of azinphosmethyl by mouse liver. Pesticide Biochemistry and Physiology. ص. 170–177.
- ^ ا ب ج د ه Petroianu, G.A (2014). Reversible cholinesterase inhibitors as pre-treatment for exposure to organophosphates: assessment using azinphos-methyl. J Appl Toxicol.
- ^ ا ب Iyer, R.؛ B. Iken؛ A. Leon (2015). "Developments in alternative treatments for organophosphate poisoning". Toxicol Lett. ج. 233 ع. 2: 200–206. DOI:10.1016/j.toxlet.2015.01.007.
- ^ Ghoshdastidar, A.J. (2012). "Membrane bioreactor treatment of commonly used organophosphate pesticides". J Environ Sci Health B. ج. 47 ع. 7: 742–750. DOI:10.1080/03601234.2012.669334.
- ^ Klaassen CD؛ A.M., Doull J (1995). Toxic effects of pesticides, in Casarett and Doull's toxicology: The basic science of poisons. McGraw-Hill Companies: New York. ص. 643–689.
- ^ Cortes-Eslava, J (2013). "The role of plant metabolism in the mutagenic and cytotoxic effects of four organophosphorus insecticides in Salmonella typhimurium and in human cell lines". Chemosphere. ج. 92 ع. 9: 1117–1125. DOI:10.1016/j.chemosphere.2013.01.058. PMID:23434078.
- ^ Buono, S. (2012). "Toxic effects of pentachlorophenol, azinphos-methyl and chlorpyrifos on the development of Paracentrotus lividus embryos". Ecotoxicology. ج. 21 ع. 3: 688–697. DOI:10.1007/s10646-011-0827-6.
- ^ Meyers, S.M.؛ J.O. Wolff (1994). "Comparative toxicity of azinphos-methyl to house mice, laboratory mice, deer mice, and gray-tailed voles". Archives of Environmental Contamination and Toxicology. ج. 26 ع. 4: 478–482. DOI:10.1007/bf00214150.
- ^ Jordaan, M.؛ S. Reinecke؛ A. Reinecke (2012). "Acute and sublethal effects of sequential exposure to the pesticide azinphos-methyl on juvenile earthworms (Eisenia andrei)". Ecotoxicology. ج. 21 ع. 3: 649–661. DOI:10.1007/s10646-011-0821-z.
- ^ Kimmerle, G. (1976). "Subchronic inhalation toxicity of azinphos-methyl in rats". Archives of Toxicology. ج. 35 ع. 2: 83–89. DOI:10.1007/bf00372761.
- ^ Kluver, N. (2009). "Toxicogenomic response of azinphos-methyl treated zebrafish embryos and implication for the development of predictive models for chronic (fish) toxicity". Toxicology Letters. ج. 189: 94. DOI:10.1016/j.toxlet.2009.06.284.
- ^ Jordaan, M.S.؛ S.A. Reinecke؛ A.J. Reinecke (2012). "Acute and sublethal effects of sequential exposure to the pesticide azinphos-methyl on juvenile earthworms (Eisenia andrei)". Ecotoxicology. ج. 21 ع. 3: 649–661. DOI:10.1007/s10646-011-0821-z.
- ^ Jordaan, M.S.؛ S.A. Reinecke؛ A.J. Reinecke (2013). "Biomarker responses and morphological effects in juvenile tilapia Oreochromis mossambicus following sequential exposure to the organophosphate azinphos-methyl". Aquat Toxicol. 144–145: 133–140. DOI:10.1016/j.aquatox.2013.10.007.
- ^ Nebeker, A.V. (1998). "Impact of guthion on survival and growth of the frog Pseudacris regilla and the salamanders Ambystoma gracile and Ambystoma maculatum". Arch Environ Contam Toxicol. ج. 35 ع. 1: 48–51. DOI:10.1007/s002449900347.
- ^ Ferrari, A (2011). "Effects of azinphos methyl and carbaryl on Rhinella arenarum larvae esterases and antioxidant enzymes". Comp Biochem Physiol C. ج. 153 ع. 1: 34–39. DOI:10.1016/j.cbpc.2010.08.003.
- ^ Ferrari, A.؛ A. Venturino؛ A.M. Pechen de D'Angelo (2007). "Muscular and brain cholinesterase sensitivities to azinphos methyl and carbaryl in the juvenile rainbow trout Oncorhynchus mykiss". Comp Biochem Physiol C. ج. 146 ع. 3: 308–313. DOI:10.1016/j.cbpc.2007.04.002.
- ^ Ferrari, A. (2004). "Different susceptibility of two aquatic vertebrates (Oncorhynchus mykiss and Bufo arenarum) to azinphos methyl and carbaryl". Comp Biochem Physiol C. ج. 139 ع. 4: 239–243. DOI:10.1016/j.cca.2004.11.006.
- ^ Morton, M.G (1997). "Acute and chronic toxicity of azinphos-methyl to two estuarine species, Mysidopsis bahia and Cyprinodon variegatus". Arch Environ Contam Toxicol. ج. 32 ع. 4: 436–441. DOI:10.1007/s002449900210.
- ^ Wauchope, R.D (1992). "The SCS/ARS/CES pesticide properties database for environmental decision-making". Rev Environ Contam Toxicol. ج. 123: 1–155.