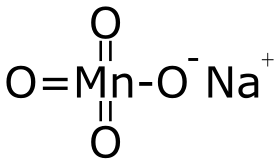بيرمنغنات الصوديوم
مركب كيميائي
فوق منغنات الصوديوم أو بيرمنغنات الصوديوم مركب كيميائي له الصيغة NaMnO4 ، ويكون على شكل بلورات حمراء بنفسجية . عدد أكسدة المنغنيز في هذا المركب +7 ، وهو من المؤكسدات القوية.
| بيرمنغنات الصوديوم | |
|---|---|
| أسماء أخرى | |
بيرمنغنات صوديوم |
|
| المعرفات | |
| رقم CAS | 10101-50-5 |
| بوب كيم | 23673458 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
| الخواص | |
| الصيغة الجزيئية | NaMnO4 |
| الكتلة المولية | 141.93 غ/مول (لا مائي) 159.94 غ/مول (أحادي هيدرات) |
| المظهر | بلورات حمراء بنفسجية |
| الكثافة | 1.972 غ/سم3 (أحادي هيدرات) |
| الذوبانية في الماء | منحل بشكل جيد |
| المخاطر | |
| ترميز المخاطر | |
| توصيف المخاطر | |
| تحذيرات وقائية | |
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
الخواص
عدل- يشبه مركب فوق منغنات الصوديوم بخواصه المؤكسدة مركب فوق منغنات البوتاسيوم المستخدم بشكل أكبر، وذلك لانخفاض سعره بالمقارنة مع فوق منغنات الصوديوم.
- انحلالية مركب فوق منغنات الصوديوم كبيرة جداً، وله خاصة استرطاب كبيرة أيضاً.
- يتفكك فوق منغنات الصوديوم بالتسخين مطلقاً غاز الأكسجين.
التحضير
عدليحضر عن طريق فوق منغنات البوتاسيوم، ولا يحضر بشكل مباشر من تفاعل ثنائي أكسيد المنغنيز مع هيدروكسيد الصوديوم، وذلك بسبب عدم تشكل ملح Na2MnO4 الوسطي الضروري لعملية التحضير.
الاستخدامات
عدل- لا يستخدم بشكل مكثف في الكيمياء التحليلية مثل فوق منغنات البوتاسيوم بسبب تميه البلورات بسبب الاسترطاب.
- بسبب خواصه المؤكسدة القوية وانحلاليته العالية تستعمل محاليله المائية في تخريش اللوح أثناء تحضير اللوحة الإلكترونية المطبوعة.[2]
منغنات الصوديوم
عدلمنغنات الصوديوم وهو مركب له الصيغة Na2MnO4 حيث للمنغنيز رقم أكسدة +6، وهو على شكل بلورات خضراء وله كتلة مولية مقدارها 141.93 غ/مول. يحضر من تفاعل ثنائي أكسيد المنغنيز مع هيدروكسيد الصوديوم بدرجات حرارة مرتفعة. كما ينتج من تفاعل اختزال فوق منغنات الصوديوم بشروط قاعدية حسب المعادلة:
- 4NaOH + 4NaMnO4 → 4Na2MnO4 + 2H2O + O2
المراجع
عدل- ^ ا ب ج SODIUM PERMANGANATE (بالإنجليزية), QID:Q278487
- ^ Arno H. Reidies "Manganese Compounds" in Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim. دُوِي:10.1002/14356007.a16_123