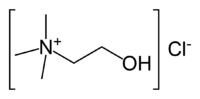
كلوريد الكولين
كلوريد الكولين مركب عضوي صيغته الكيميائية [(CH3) 3NCH2CH2OH] Cl. إنه ثنائي الوظيفة ، يحتوي على ملح الأمونيوم الرباعي والكحول. الكاتيون هو مادة الكولين التي تحدث بشكل طبيعي. وهو ملح أبيض قابل للذوبان في الماء يستخدم بشكل أساسي في علف الحيوانات.[2]
| كلوريد الكولين | |
|---|---|
| التسمية المفضلة للاتحاد الدولي للكيمياء البحتة والتطبيقية | |
2-Hydroxy-N,N,N-trimethylethan-1-aminium chloride |
|
| أسماء أخرى | |
|
|
| المعرفات | |
| رقم CAS | 67-48-1 |
| بوب كيم (PubChem) | 522265 |
مواصفات الإدخال النصي المبسط للجزيئات
|
|
|
|
| الخواص | |
| صيغة كيميائية | C5H14ClNO |
| كتلة مولية | 139.62 غ.مول−1 |
| المظهر | بلورات بيضاء أو ديليكيسسينت |
| نقطة الانصهار | 302 °س، 575 °ك، 576 °ف |
| الذوبانية في الماء | very soluble (>650 g/l)[1] |
| المخاطر | |
| NFPA 704 |
|
| في حال عدم ورود غير ذلك فإن البيانات الواردة أعلاه معطاة بالحالة القياسية (عند 25 °س و 100 كيلوباسكال) | |
| تعديل مصدري - تعديل | |
تركيب
عدلفي المختبر ، يمكن تحضير الكولين عن طريق مثيلة ثنائي ميثيل إيثانولامين مع كلوريد الميثيل.
يتم إنتاج كلوريد الكولين بكميات كبيرة حيث يقدر الإنتاج العالمي بنحو 160 ألف طن في عام 1999.[2] صناعيًا ، يتم إنتاجه عن طريق تفاعل أكسيد الإيثيلين ، وكلوريد الهيدروجين ، وثلاثي ميثيل أمين، [3] أو من ملح المُشكل مسبقًا:[4]
التطبيقات
عدلوهي مادة مضافة مهمة في الأعلاف وبالأخص العلف المخصص للدجاج حيث تسرع النمو. وهو يشكل مذيبًا سهل الانصهار مع اليوريا والإيثيلين جلايكول والجلسرين والعديد من المركبات الأخرى.
كما أنها تستخدم كمادة مضافة للتحكم في الصلصال في السوائل المستخدمة في التكسير الهيدروليكي.[5]
الأملاح ذات الصلة
عدلالأملاح التجارية الأخرى الكولين هي هيدروكسيد الكولين وكولين بيطرطرات. في المواد الغذائية ، غالبًا ما يوجد المركب في صورة فسفاتيديل كولين.
المراجع
عدل- ^ "Chemical Safety Information from Intergovernmental Organizations - Choline Chloride" (PDF). مؤرشف من الأصل (PDF) في 2017-07-12.
- ^ ا ب Matthias Frauenkron, Johann-Peter Melder, Günther Ruider, Roland Rossbacher, Hartmut Höke (2002). "Ethanolamines and Propanolamines". Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. DOI:10.1002/14356007.a10_001. ISBN:3527306730.
- ^ title= Johnson Matthey Process Technology - Choline chloride licensed process
- ^ "Choline chloride" (PDF). Screening Information Data Set (SIDS) for High Production Volume Chemicals. IPCS INCHEM. مؤرشف من الأصل (PDF) في 2017-07-12. اطلع عليه بتاريخ 2009-11-10.
- ^ "What Chemicals Are Used". FracFocus. مؤرشف من الأصل في 2020-07-02. اطلع عليه بتاريخ 2014-09-19.